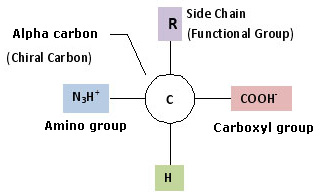
Свойствата на α-аминокиселините са сложни, но опростени, тъй като всяка молекула на аминокиселина включва две функционални групи: карбоксилна (-COOH) и амино (-NH2).
Всяка молекула може да съдържа странична верига или R група, например аланинът е пример за стандартна аминокиселина, съдържаща метилова група на страничната верига.R групите имат различни форми, размери, заряди и реактивност.Това позволява аминокиселините да бъдат групирани според химичните свойства на техните странични вериги.
Таблица с общи съкращения и свойства на аминокиселини
| Име | Трибуквен код | Еднобуквен код | Молекулярна | Молекулярна | остатък | Остатъчно тегло | pKa | pKb | pKx | pl |
| Аланин | Ала | A | 89.10 | C3H7NO2 | C3H5NO | 71.08 | 2.34 | 9,69 | – | 6.00 |
| Аргинин | Арг | R | 174.20 | C6H14N4O2 | C6H12N4O | 156.19 | 2.17 | 9.04 | 12.48 | 10.76 |
| Аспарагин | Asn | N | 132.12 | C4H8N2O3 | C4H6N2O2 | 114.11 | 2.02 | 8,80 | – | 5.41 |
| Аспарагинова киселина | Asp | D | 133.11 | C4H7NO4 | C4H5NO3 | 115.09 | 1,88 | 9.60 | 3,65 | 2.77 |
| цистеин | Cys | C | 121.16 | C3H7NO2S | C3H5NOS | 103.15 | 1,96 | 10.28 | 8.18 | 5.07 |
| Глутаминова киселина | Glu | E | 147.13 | C5H9NO4 | C5H7NO3 | 129.12 | 2.19 | 9,67 | 4.25 | 3.22 |
| Глутамин | Gln | Q | 146.15 | C5H10N2O3 | C5H8N2O2 | 128.13 | 2.17 | 9.13 | – | 5,65 |
| Глицин | Гли | G | 75.07 | C2H5NO2 | C2H3NO | 57.05 | 2.34 | 9.60 | – | 5,97 |
| Хистидин | Неговата | H | 155.16 | C6H9N3O2 | C6H7N3O | 137.14 | 1.82 | 9.17 | 6.00 | 7.59 |
| Хидроксипролин | Hyp | O | 131.13 | C5H9NO3 | C5H7NO2 | 113.11 | 1.82 | 9,65 | – | – |
| Изолевцин | Ил | I | 131.18 | C6H13NO2 | C6H11NO | 113.16 | 2.36 | 9.60 | – | 6.02 |
| левцин | лев | L | 131.18 | C6H13NO2 | C6H11NO | 113.16 | 2.36 | 9.60 | – | 5,98 |
| Лизин | Lys | K | 146.19 | C6H14N2O2 | C6H12N2O | 128.18 | 2.18 | 8,95 | 10.53 | 9,74 |
| Метионин | Мет | M | 149.21 | C5H11NO2S | C5H9NOS | 131.20 | 2.28 | 9.21 | – | 5.74 |
| Фенилаланин | Phe | F | 165.19 | C9H11NO2 | C9H9NO | 147.18 | 1.83 | 9.13 | – | 5.48 |
| Пролин | Професионалист | P | 115.13 | C5H9NO2 | C5H7NO | 97.12 | 1,99 | 10.60 | – | 6.30 |
| Пироглутаматичен | Glp | U | 139.11 | C5H7NO3 | C5H5NO2 | 121.09 | – | – | – | 5.68 |
| серин | сер | S | 105.09 | C3H7NO3 | C3H5NO2 | 87.08 | 2.21 | 9.15 | – | 5.68 |
| Треонин | Thr | T | 119.12 | C4H9NO3 | C4H7NO2 | 101.11 | 2.09 | 9.10 | – | 5.60 |
| Триптофан | Trp | W | 204.23 | C11H12N2O2 | C11H10N2O | 186.22 | 2.83 | 9.39 | – | 5,89 |
| Тирозин | Тир | Y | 181.19 | C9H11NO3 | C9H9NO2 | 163.18 | 2.20 | 9.11 | 10.07 | 5.66 |
| Валин | Вал | V | 117.15 | C5H11NO2 | C5H9NO | 99.13 | 2.32 | 9.62 | – | 5,96 |
Аминокиселините са кристални твърди вещества, които обикновено са водоразтворими и само умерено разтворими в органични разтворители.Тяхната разтворимост зависи от размера и природата на страничната верига.Аминокиселините имат много високи точки на топене, до 200-300°C.Другите им свойства варират за всяка отделна аминокиселина.
Време на публикуване: 19 април 2021 г





